重金属捕集剂法处理低浓度电镀废水
0 引 言
近年来,随着电镀工业的不断发展,尤其是点多面广的乡镇电镀企业的迅速发展,电镀行业的污染扩散面积不断扩大,电镀废水成为具有代表性的难处理工业废水之一[1].目前重金属处理技术虽然种类很多,如化学沉淀、化学氧化还原、膜分离、离子交换等,但出于经济性、操作性、维护性等方面的考虑,当前国内绝大多数的电镀企业均采用化学沉淀法处理电镀废水,其中又以碱性沉淀处理居多[2-6].然而,随着新的《电镀污染物排放标准》(GB 21900-2008)的正式实施,经传统化学方法处理的出水已无法完全达到新标准的排放要求.在这种情况下,重金属捕集剂法由于其良好的处理效果成为电镀废水末端处理的理想选择.但目前市场上重金属捕集剂种类繁多,其在处理效率和经济性等方面尚未有系统的分析评估,给该法的工业化应用造成了一定的影响.因此,本文对市场上常见的重金属捕集剂进行了筛选并对其用于低浓度电镀废水处理进行了研究.
1 试验部分
1.1 仪器与试剂
试验仪器: TAS-990原子吸收分光光度计、PHS-25C酸度计、85-2恒温磁力搅拌器、PA-200分析天平.配制重金属模拟废水所用试剂:NiSO4·6H2O,Cr2(SO4)3·6H2O,CuSO4·5H2O,C10H16N2O8Na2·H2O,Na4P2O7·10H2O,以上试剂均为分析纯.重金属捕集剂:DTCR、CM-1、MCP、TMTB和TMTF,市场上采购.
1.2 试验方法
取200 mL模拟废水于250 mL烧杯中,调节pH值,加入一定量的金属捕集剂,置于恒温磁力搅拌器上搅拌5 min,然后静置15 min,取上清液,用原子吸收分光光度法测定上清液中金属离子浓度.
1.3 试验原理
以DTCR为例,DTCR为一种液状二硫代氨基甲酸型螯合剂,含有大量的极性基(极性基中的硫原子半径较大、带负电,且易于极化变形而产生负电场),它能捕捉阳离子并趋向成键而生成难溶的二硫代氨基甲酸(DTC)盐.生成的DTC盐有部分是离子键或强极性键(如DTC-Ag),大多数是配价键(如DTC-Cu、DTC-Zn、DTC-Fe).同一金属离子螯合的配价基极可能来自不同的DTCR分子,这样生成的DTC盐分子会是高交联、立体结构的,原DTCR的相对分子质量为(10-15)×104,而生成的难溶螯合盐的相对分子质量可达数百万甚至上千万,故此种金属盐一旦在水中生成,便有很好的絮凝沉淀效果[7].
2 结果与讨论
2.1 捕集剂的筛选
Ni2+浓度为1.0 mg·L-1的模拟废水,pH值调为8.0.因为根据Ni(OH)2的溶度积计算,pH>8.7时Ni2+产生沉淀,而且传统化学沉淀出水一般为碱性.分别用DTCR、MCP、TMTB、TMTF及CM-1重金属捕集剂对模拟废水进行处理,捕集剂投加量为各自理论投加量的1.2倍(所需的DTCR、CM-1、MCP、TMTB和TMTF的理论投加量分别为0.12、0.11、0.12、0.10 mL和0.10 mL,此数据由试剂供应商提供),实验结果见表1.由表1可知,CM-1、MCP和TMTB均能使含Ni2+废水达标排放,其中CM-1处理效果最好.
 |
根据各捕集剂市场价格及用量,计算处理单位废水时所需的成本,结果如表2所示.由表2知,相对MCP和TMTB,CM-1的处理成本最低.综合以上,CM-1是最适用于处理低浓度含镍废水的重金属捕集剂.
接着,用CM-1分别处理含Cr3+、EDTA-Cu和焦磷酸铜的模拟废水,水样中金属离子浓度均为1.0 mg·L-1,pH值为8.0,捕集剂投加量为1.2倍理论投加量,实验结果如表3所示.由表3知,在对含Cr3+、EDTA-Cu和焦磷酸铜的废水处理中CM-1同样表现出良好的去除重金属的性能.综上,CM-1是处理低浓度电镀废水的最佳选择.
 |
2.2 捕集剂投加量对处理效果的影响
用CM-1分别处理含Ni2+、Cr3+、EDTA-Cu和焦磷酸铜的模拟废水,水样中金属离子浓度均为1.0 mg·L-1,pH值为8.0,分别在0.6、0.8、1.0、1.2、1.5、2.0倍理论投加量的条件下进行实验,结果如图1所示.
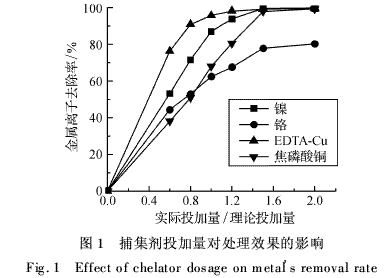 |
由图1可以看出,随着CM-1投加量的增加,重金属的去除率也不断升高.当投加量为理论投加量的1.2倍左右时,Ni2+和EDTA-Cu的去除率达到最大值;当投加量为理论投加量的1.5倍左右时,Cr3+和焦磷酸铜的去除率达到最大值.当投加量继续增大时,去除率保持稳定.其中Ni2+、EDTA-Cu和焦磷酸铜的去除率能达到99%左右,而Cr3+的去除效果相对差一些,最高去除率仅接近80%.
2.3 pH值对处理效果的影响
在最佳捕集剂投加量下,对含Ni2+、Cr3+、ED-TA-Cu和焦磷酸铜的模拟废水进行pH值对处理效果的影响实验.由于传统化学沉淀出水一般为碱性,故选定pH值范围为7~11.实验结果如图2所示.
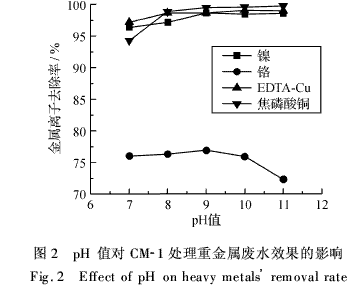 |
由图2分析可知,当pH值在7~9时,各金属离子的去除率均随着pH值的增大而增大;pH值继续增大时,Ni2+、EDTA-Cu和焦磷酸铜的去除率保持不变,而Cr3+的去除率反而下降.这主要是因为在pH值为7~9时,游离的金属离子以碱性沉淀的方式被去除;两性离子Cr3+在较高pH值条件下生成多羟基化合物,而CM-1可能对多羟基化合物的螯合沉淀能力较差,导致了去除率的下降.
2.4 废水初始浓度对处理效果的影响
改变废水初始浓度,在各自最佳pH值条件下,对含Ni2+、Cr3+、EDTA-Cu和焦磷酸铜的模拟废水分别进行处理,得到不同初始浓度条件下去除率随投加量的变化曲线,如图3~6所示.
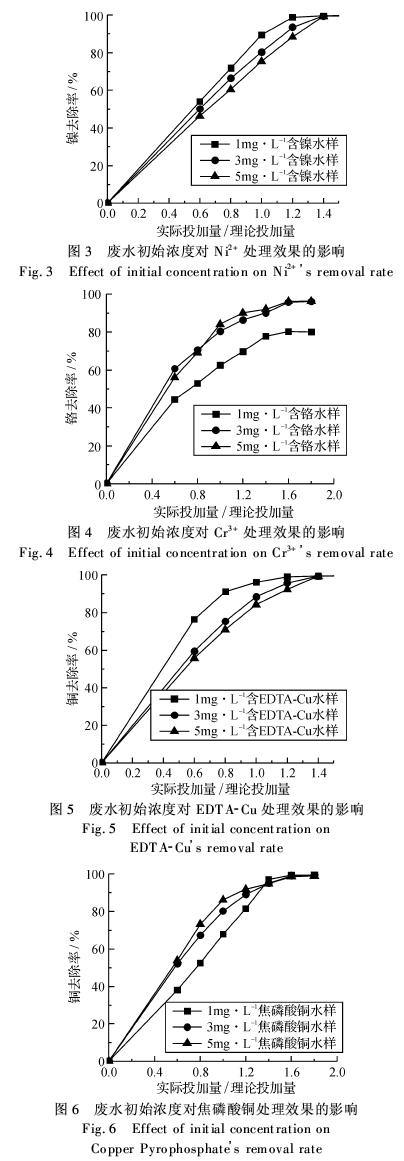 |
分析各图可知,对于Ni2+和EDTA-Cu,废水初始浓度为1.0 mg·L-1时,最佳投加量为理论投加量的1.2倍左右,初始浓度为5.0 mg·L-1时,最佳投加量是理论投加量的1.4倍左右,初始浓度为3.0 mg·L-1时,最佳投加量为理论投加量的1.2~1.4倍.类似,对于Cr3+和焦磷酸铜,其废水初始浓度为1.0、3.0、5.0 mg·L-1时的捕集剂最佳投加量分别为1.5倍、1.5~1.6倍和1.6倍的理论投加量.
上述结果表明,随着废水初始浓度的增加,捕集剂最佳投加量相对于其理论投加量的倍数稍有增加,因而CM-1比较适用于低浓度重金属废水的处理.
此外,Cr3+的去除规律和其他几种金属离子稍有不同,Cr3+初始浓度为1.0 mg·L-1时去除率相对较低,可能原因是CM-1对三价金属离子的螯合能力相对较弱,只能将金属离子浓度降到某一程度,故初始浓度低的去除率反而较低.
2.5 金属离子共存对处理效果的影响
对含Ni2+、Cr3+、EDTA-Cu和焦磷酸铜的混合模拟废水进行处理,水样中各金属离子浓度均为1.0 mg·L-1,pH值为8.0,改变捕集剂投加量,得到各金属去除率同投加量的变化曲线,如图7所示.
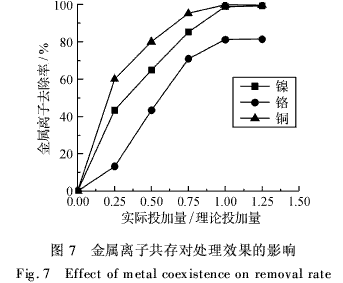 |
由图7可知,铜、镍、铬的去除率均随着投加量的加大而上升,当投加量达理论投加量时,各金属去除率便已达最大值,此时的投加量远小于单独处理4种废水所需的最佳投加量之和,可见离子共存对重金属的去除起到了促进作用.这可能由表面吸附、包藏、生成混晶等原因造成.
其次,在最大去除率上,几种重金属离子共存和其单独存在时差别不是很大,但Cr3+的去除率有一定程度的上升,其主要原因是在表面吸附过程中,离子价数越高,其越容易被吸附.
此外,铜的去除率始终高于其他两种金属,镍的去除率次之,Cr3+的去除率最低.该结果表明,CM-1对不同重金属的螯合能力并不相同,其顺序为铜>镍>铬.
2.6 捕集剂CM-1成分分析 在500~4 000 cm-1,对CM-1进行红外光谱测定,确定其主要官能团及物质类别.在200~400 nm,以水为溶剂,对CM-1进行紫外-可见光谱测定,进一步确定其类别.图8和图9分别是CM-1的红外光谱扫描曲线和紫外光谱扫描曲线.
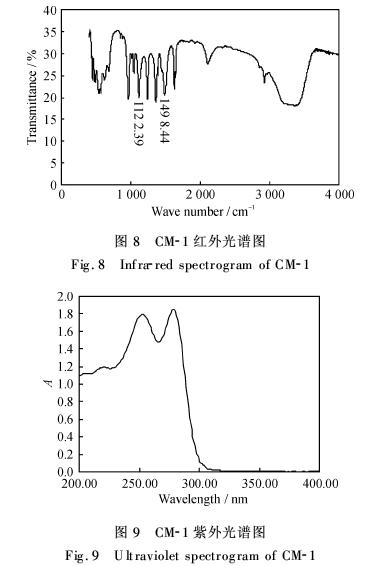 |
图8中在1 498.44 cm和1 122.39 cm处有两个强的吸收峰,其中前者为二硫代氨基甲酸盐中碳氮键伸缩振动吸收,该峰处在C—N单键(1 300 cm-1)和C N双键(1 600 cm-1)之间,具有较大双键性质,后者为碳硫键特征吸收,其峰低于C S双键(1 200~1 500 cm-1).上述特征表明CM-1为DTC类物质.
图9中在255 nm和280 nm附近均存在最大吸收,其中,255 nm处为N—C—S基团的π-π*跃迁,280 nm处为S—C—S基上硫原子上非键电子向共轭体系的n-π*跃迁[8],这再一次证明了碳氮和碳硫之间具有部分双键的结构特征,确定其为DTC类物质.
3 结 论
(1)经筛选试验得知,相对于市场上其他常见的重金属捕集剂,CM-1不仅对低浓度电镀废水中较难达标的游离态和络合态的重金属都具有较好的去除效果,出水能达到新标准的排放要求,而且在处理成本上也显示出较大的优越性,是一种理想的重金属捕集剂,具有较好的应用前景.
(2)在处理低浓度电镀废水过程中,捕集剂投加量、废水pH值、废水初始浓度和金属离子共存等因素都会对处理效果产生一定的影响.①在废水浓度为1.0 mg·L-1时,处理含Ni2+和EDTA-Cu废水的捕集剂最佳投加量为1.2倍的理论投加量,处理含Cr3+和焦磷酸铜废水的捕集剂最佳投加量为1.5倍的理论投加量.②较高的pH值对处理含Ni2+、EDTA-Cu和焦磷酸铜的废水较为有利,pH>9对Cr3+的去除不利.③废水初始浓度升高时,所需的捕集剂用量相对其理论投加量的倍数略有增加,因而CM-1用于处理低浓度电镀废水时比较经济.④金属离子共存能提高处理效果,在较小捕集剂用量下即能达到去除要求,CM-1对不同金属的螯合能力不同,表现为铜>镍>铬.
(3)建议使用方法:先采用传统化学沉淀法处理电镀废水,使重金属离子降至一定浓度后再采用捕集剂法,这样可以保证处理出水达标,同时经济成本也较低.
参考文献:
[1] 周东晓,鲁宪,支宗琦,等.电镀行业污染物产生与防治措施[J].科技资讯,2008,(14):224-225.
[2]XU Ying, ZHANG Fang. Experimental research onheavy metal
wastewater treatment with dipropyl di-thiophosphate[J].J of Hazardous
Materials,2006,137:1636-1642.
[3] 马前,张小龙.国内外重金属废水处理新技术的研究进展[J].环境工程学报,2007,1(7):10-14.
[4] 张志军,李玲,朱宏,等.化学沉淀法去除电镀废水中铬的实验研究[J].环境科学与技术,2008,31(7):96-97.
[5] 谢少雄,黄功浩,黄美燕.铁屑法处理电镀含铬废水的试验及应用[J].工业水处理,2003,23(6):28-30.
[6] 崔春花,张卫东,任钟旗,等.中空纤维更新液膜技术处理模拟含铜电镀废水[J].电镀与涂饰,2009,28(3):31-33.
[7] 王文丰.螯合沉淀法处理电镀废水的工业实践[J].环境污染治理技术与设备,2005,6(9):83-85.
[8] 许海峰,唐瑞仁,曹佐英,等.壳聚糖黄原酸盐对Cu2+的吸附性能[J].应用化学,2008,25(6):673-676.(责任编辑 涂 红)

使用微信“扫一扫”功能添加“谷腾环保网”








